组蛋白乙酰化修饰是细胞表观遗传调控的主要方式之一,在基因转录、DNA复制和DNA损伤修复等过程中至关重要,该化学修饰受到组蛋白乙酰转移酶(histone acetyltransferases, HATs)和组蛋白去乙酰化酶(histone deacetylases, HDACs)的动态调控。E1A相关蛋白p300(p300, EP300, KAT3B)和环磷酸腺苷反应元件结合蛋白(CBP, CREBBP, KAT3A)是一对旁系同源的组蛋白乙酰转移酶和转录共激活因子,它们通过对基因启动子和增强子H3K18和H3K27位点以及多种转录因子的乙酰化激活基因转录。p300/CBP对增强子的异常激活导致癌基因表达上调,通过改变细胞周期调控、细胞自噬等过程促进癌症发生发展。目前,靶向p300/CBP的抗肿瘤策略主要包括p300/CBP催化结构域和溴结构域抑制剂,已有数个抑制剂处于临床试验阶段,主要适应症为多种血液肿瘤和去势抵抗性前列腺癌。
yl34511线路中心李英霞教授课题组近年来致力于新型p300/CBP抑制剂发现,报道了多个p300/CBP催化结构域抑制剂和溴结构域抑制剂(Eur. J. Med. Chem. 2019, 180, 171–190, Bioorg. Chem. 2022, 124, 105803, Bioorg. Med. Chem. 2022, 66, 116784),并研究了它们的抗肿瘤活性和机制。
近日,李英霞教授课题组与临港实验室黄洵研究员课题组合作在药物化学专业期刊《Journal of Medicinal Chemistry》上发表了题为“Discovery of Novel PROTAC Degraders of p300/CBP as Potential Therapeutics for Hepatocellular Carcinoma”的研究论文,报道了新型p300/CBP PROTAC降解剂QC-182及其潜在的抗肝细胞癌活性和机制。
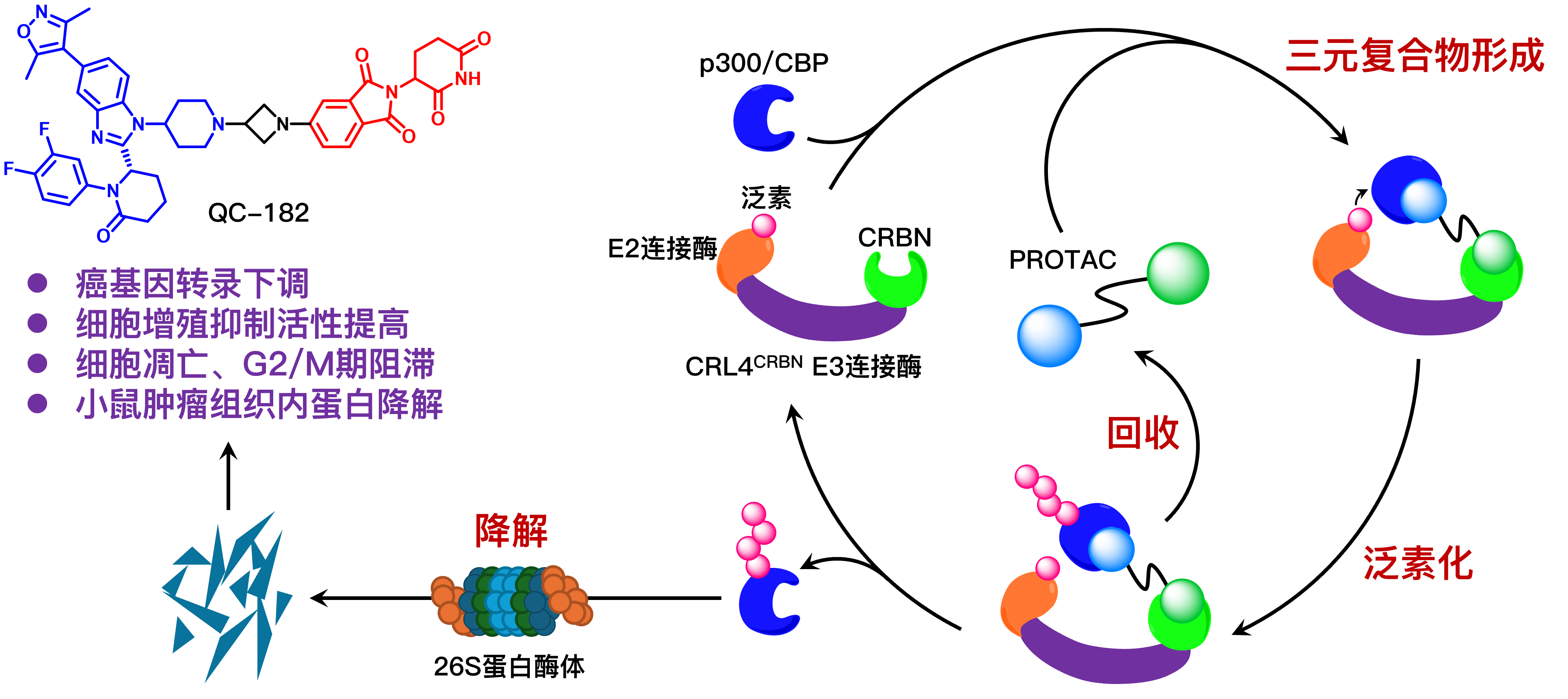
研究表明,p300/CBP除催化结构域和溴结构域外,其他结构域也参与癌基因转录激活;此外,p300/CBP催化结构域和溴结构域抑制剂的联合给药具有更高的抗肿瘤活性。因此,通过基于蛋白降解靶向嵌合体(proteolysis-targeting chimera, PROTAC)的蛋白降解策略,有望实现更强效的抗肿瘤作用。另外,由于靶向p300/CBP的实体瘤适应症研究不足,研究团队前期进行了敏感肿瘤细胞筛选,确定肝细胞癌为本研究的目标适应症。
本研究选择临床试验进展最快的p300/CBP溴结构域抑制剂CCS1477作为构建靶向p300/CBP PROTAC降解剂的靶蛋白配体原型,通过复合物晶体结构分析结合生化实验检测,确定并验证了合适的接头位点,从而进行PROTAC分子的构建和肝细胞癌细胞中的靶蛋白降解活性筛选,最终得到了优选p300/CBP PROTAC降解剂QC-182。该分子能够通过PROTAC作用机制有效降解SK-HEP-1细胞中的p300和CBP蛋白。经测序分析发现,QC-182可显著下调p300/CBP调控的转录组水平,特别是参与上皮−间质转化和G2/M期检查点的癌基因转录。QC-182相比于原型抑制剂CCS1477和近期报道的降解剂dCBP-1具有更显著的抗增殖活性,同时可诱导细胞凋亡和G2/M期阻滞。小鼠体内研究结果发现,QC-182可降解SK-HEP-1小鼠肿瘤组织中的p300和CBP蛋白。综上,QC-182是一种有效的p300/CBP PROTAC降解剂,进一步优化有望得到抑制肝细胞癌和其他实体瘤生长的先导化合物。
yl34511线路中心药物化学系2020级博士研究生唱祺、中国科学院上海药物研究所硕士研究生李佳怡、邓玥为本论文的共同第一作者,yl34511线路中心李英霞教授和临港实验室黄洵研究员为本论文的通讯作者。该研究工作得到了国家自然科学基金委、上海市科委的项目资助。
原文链接:https://pubs.acs.org/doi/10.1021/acs.jmedchem.3c01468


